近日��,北京農學院動物科學技術學院王相國副教授課題組在《國際生物大分子雜志》(International Journal of Biological Macromolecules)上在線發表了題為《CREG1靶向結合IGF2R促進牛胎盤滋養層細胞外泌體的形成與釋放并伴隨外泌體運輸參與胎盤類器官的分化調節》(CREG1 promotes bovine placental trophoblast cells exosome release by targeting IGF2R and participates in regulating organoid differentiation via exosomes transport)的研究論文����。

胎盤是哺乳動物妊娠期間連接胎兒和母親的紐帶���。胎盤的正常生長和功能發揮是保證妊娠成功的關鍵����。反復流產、胎兒生長受限���、子癇前期等妊娠常見病均與胎盤早期發育缺陷有關。滋養層細胞是胎盤組織重要的組成細胞�����,通過分化為不同功能的細胞類型建立胎兒與母親之間的有效接觸��。因此�,胎盤滋養層細胞的早期增殖和分化是胎盤形成的關鍵事件����,且受多種基因的調控。
外泌體是妊娠期胎盤細胞分泌的一種細胞間通訊介質����,其發生和釋放受多種分泌糖蛋白的調控��。CREG1是一種廣泛表達于機體各器官組織的分泌型糖蛋白,具有抑制細胞增殖���、促進細胞分化的作用。IGF2R是一種由母體等位基因編碼的跨膜多功能糖蛋白�,位于細胞表面�,同樣參與調節細胞生長和分化�。研究證實�����,CREG1通過與IGF2R結合抑制人胚胎癌細胞的增殖�����。此外,CREG1還參與內吞作用和內體溶酶體的分選和轉運進程。
奶牛胎盤屬于子葉型胎盤,由胎兒尿囊絨毛膜和羊膜絨毛膜形成的子葉和子宮內膜上皮形成的子宮肉阜兩部分組成胎盤叢���。研究團隊發現,在奶牛胎盤早期發育過程中,CREG1�����、IGF2R和外泌體標記蛋白主要表達在胎盤子葉滋養層細胞中�,表達量隨著妊娠月份的增加而增加。過表達Creg1基因增強了胎盤滋養層細胞來源外泌體的發生和釋放,而敲低Igf2r基因的表達不僅抑制了外泌體的發生����,還抑制了Creg1基因過表達誘導的外泌體的發生和釋放����。因此�����,IGF2R不僅是CREG1正向結合蛋白可以通過反饋調節方式調節CREG1的表達���。研究團隊同時發現�����,IGF2R能夠與Rab11結合,進而促進胎盤滋養層細胞外泌體的形成和釋放。
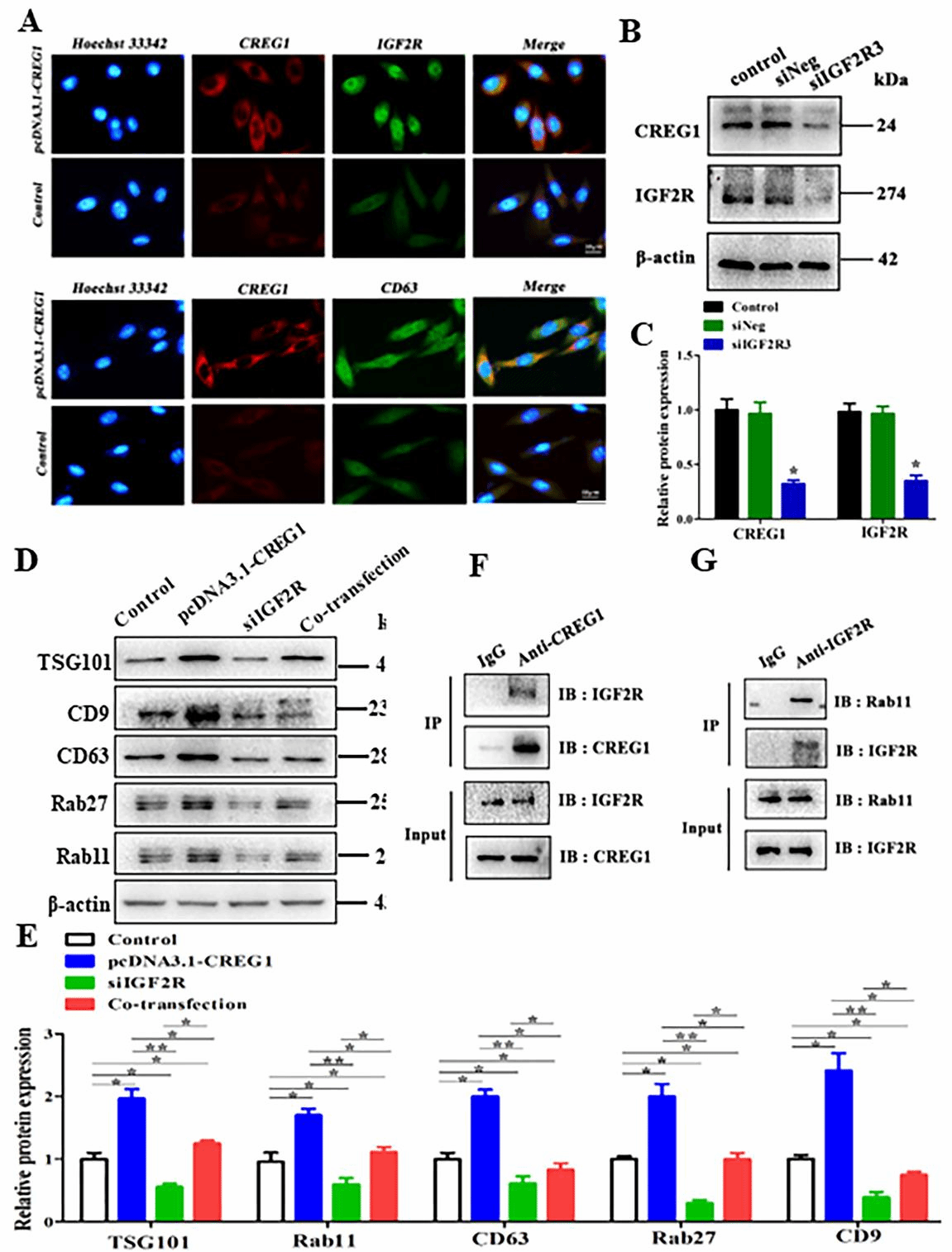
圖1 CREG1靶向結合IGF2R調控外泌體的發生和釋放
研究團隊進一步研究證實���,富含CREG1的外泌體添加入基于原代胎盤滋養層細胞構建的類器官培養基質中,至牛胎盤類器官培養的第15天,牛原代胎盤滋養層細胞衍生的類器官出現了明顯的細胞分化跡象。轉錄組分析發現���,在胎盤滋養層細胞類器官中加入富含CREG1的外泌體改變了類器官中基因的表達模式,包含胞吞作用、PI3K-Akt信號通路�����、氧化磷酸化�、蛋白質分解和吸收、內質網蛋白質加工、移植物排斥反應等�����。
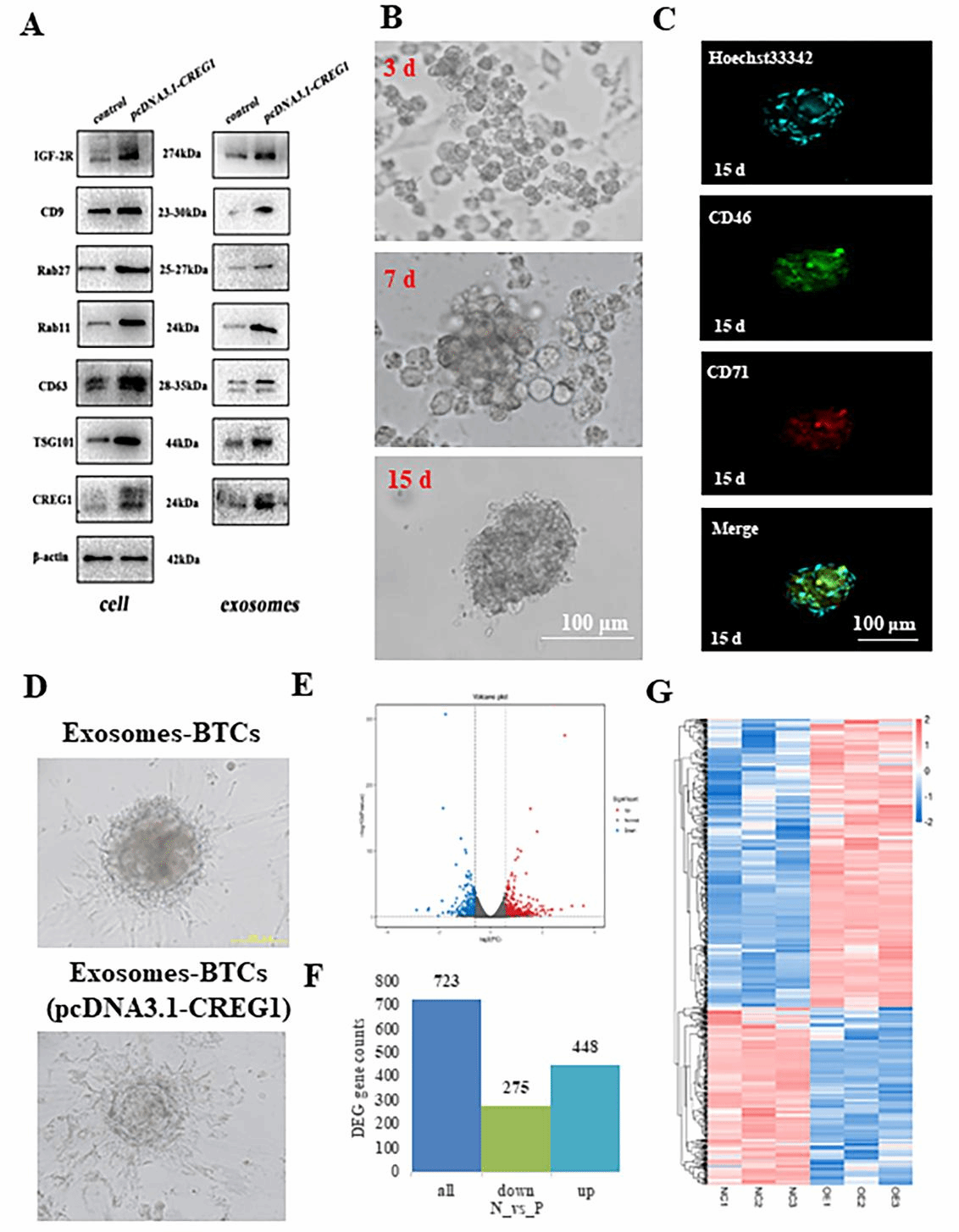
圖2 CREG1調節外泌體的發生和釋放促進牛胎盤滋養層細胞衍生類器官的分化
本研究初步闡明了CREG1調控牛妊娠早期胎盤滋養層細胞增殖分化的機制����,為胎盤早期發育缺陷的診斷和治療提供了理論和實踐依據。
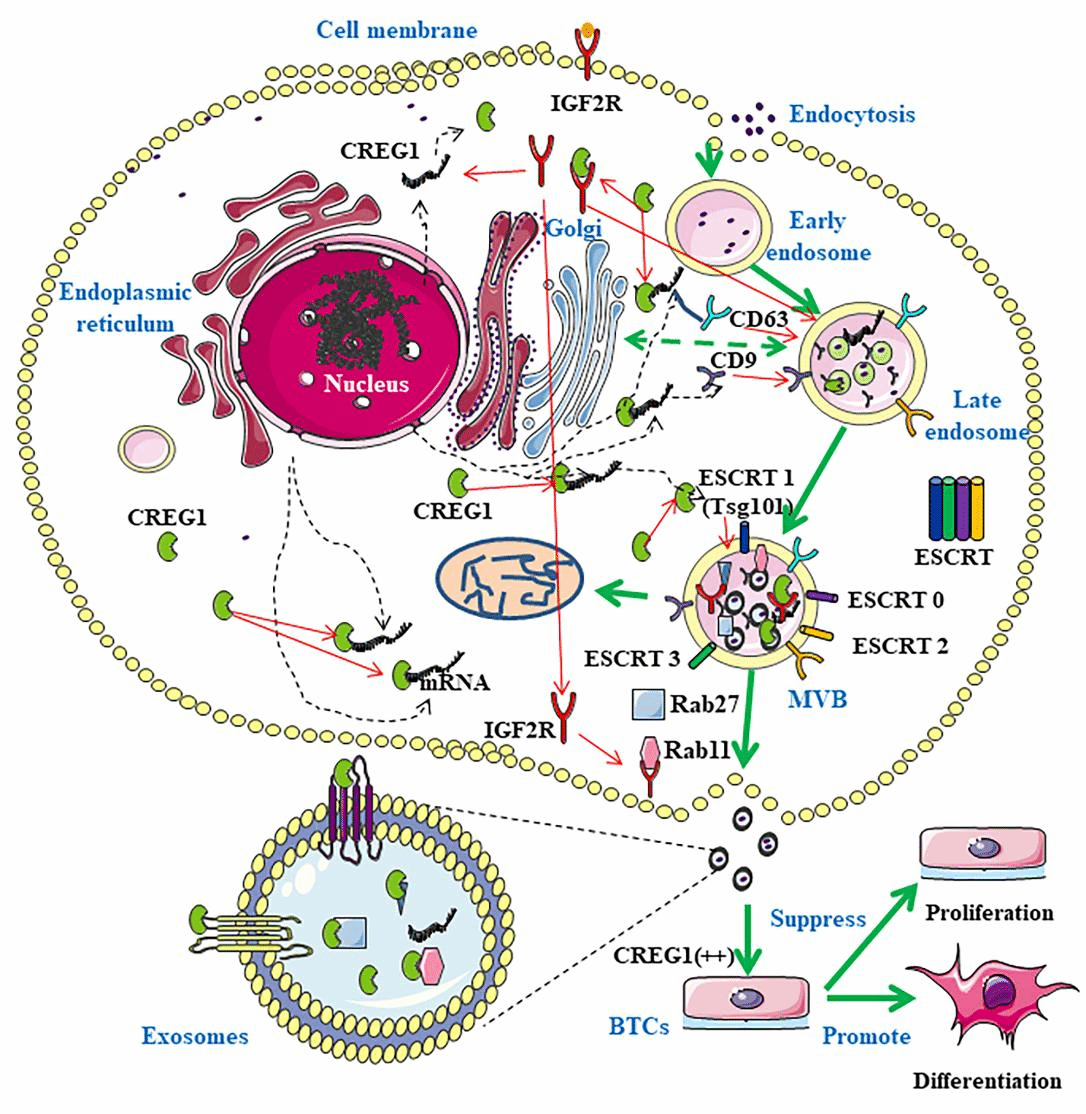
圖3 CREG1調節外泌體發生和釋放促進牛胎盤滋養層細胞衍生類器官分化模式圖
北京農學院動物科學技術學院碩士研究生袁乃涵、青年教師肖龍菲博士為論文的共同第一作者��,王相國副教授為該論文的通訊作者,盛熙暉教授�、齊曉龍副教授、郭凱軍教授,生物與資源環境學院劉冰穎博士,中國農業科學院北京畜牧獸醫研究所楊曉雯研究員等參與了本項工作�����。
該研究得到了國家自然科學基金面上項目(32273079)和北京農學院科技創新支撐計劃(BUA-HHXD2023)等資助��。
論文鏈接:https://www.sciencedirect.com/science/article/abs/pii/S0141813024041035

